엔케이맥스, 난치성 육종암 환자의 종양 약 80% 관해
- Author : 관리자
- Date : 22-01-27 14:15
- View : 5,500
관련링크
엔케이맥스, 난치성 육종암 환자의 종양 약 80% 관해
[2021.12.23] 엔케이맥스는 미국 FDA 동정적 사용 제도 승인을 받은 슈퍼NK(SNK01)와 키트루다(Keytruda) 병용요법 치료 환자에게서 긍정적인 결과를 얻었다고 23일 밝혔다.
동정적 사용(Compassionate Use)은 암과 같이 생명을 위협하고 장기간 또는 중증 질환의 적절한 치료 대안이 없을 때 개발 중이나 아직 판매허가를 취득하지 못한 신약 치료제의 사용을 승인하여 치료의 기회를 주는 FDA 제도이다. 최근 동정적 사용 프로그램이 적용된 개발약물들의 경우 FDA의 최종 허가관문을 통과할 가능성이 높다는 조사결과가 다수 나오고 있는 상황이다.
엔케이맥스는 현재 미국에서 진행중인 불응성 고형암 임상1상 초기에 슈퍼NK의 치료 가능성을 확인하고 동정적 사용을 승인 받은 바 있다. 이번에 공개된 데이터는 육종암의 일종인 결합조직성소원형세포종(DSRCT) 환자에 대한 슈퍼NK+키트루다의 동정적 사용으로 투여 받은 환자의 임상 결과이다.
해당 환자는 2017년 육종암을 판정 받은 32세의 남성 환자로 약 1년 반 동안 기존 화학요법으로 치료를 진행했으나 암세포가 줄어들지 않고 독성(toxicity)이 나타났다. 이후 키트루다 약물을 추가로 투여 받았지만 계속해서 암이 커지는 PD(progression disease)를 보여 16싸이클(cycle)에 치료가 중단됐던 상태였다.
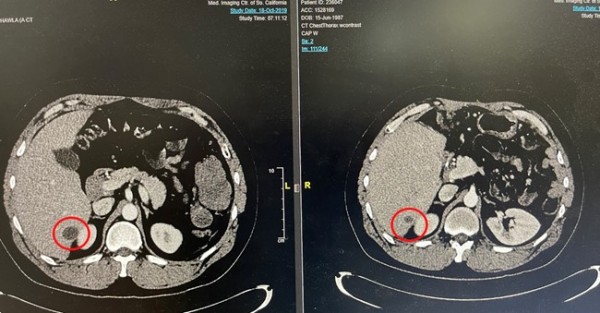
이후 이 환자는 동정적 사용 환자로 등록되어 2년간 슈퍼NK와 키트루다 병용 투여를 받았다. 그 결과, 간문에 있던 종양의 크기가 61 X 35mm에서 35 X 30mm로 줄어들었고 간의 일부분에 퍼져 있던 종양의 크기가 51 X 37 mm에서 16 X 7 mm로 감소했다. 이로써 2019년부터 2021년 11월 현재까지 간에 발생한 암의 약 78%가 사멸하는 결과를 보인 것이다.
이번 동정적 사용제도로 치료받은 환자는 미국 현지 Sarcoma Oncology Center에서 치료 받고 있다. 담당의인 차울라(Chawla) 박사는 “전이성 말기 육종암 환자들에게서 SNK01과 면역관문억제제의 병용요법에 치료효과를 보인 것은 굉장히 놀라운 일이다. 더군다나 이들은 기존 4~5차 이상의 화학치료에 실패한 환자들이다”고 말했다. “특히 동정적 사용을 통해 치료를 진행한 DSRCT 환자의 경우 2년동안의 장기간 투여에도 부작용이 전혀 없었으며, 현재 계속적인 투여를 받으며 정상적인 생활을 하고 있다”고 밝혔다. 이어 “이러한 결과는 추후 육종암에 대한 희귀의약품 개발 및 허가에 중요한 지표가 될 수 있다”며 기대감을 드러냈다.
육종암은 지난 수십년간 기존 화학치료 조합으로는 변화가 없으며, 면역관문 억제제인 바벤시오와 임핀지에 대한 각 임상결과에서도 치료반응률(PR+CR, ORR)이 0%가 나온 악성 종양이다. 현 시점에서 사실상 적절한 치료제가 없는 상황이며, 미국에서는 발병 환자수 20만명 미만으로 희귀암으로 지정되어 있다. 특히 미국에서 희귀의약품으로 지정될 경우 세액 공제, 허가심사 수수료 감면, 동일계열 제품 중 처음으로 시판허가 승인 시 7년간 독점권을 부여하는 등 다양한 혜택을 받을 수 있을 수 있는 것으로 알려져 있다.
엔케이맥스의 박상우 대표는 “이번 동정적 사용 데이터를 통해 약물의 우수성 확인은 물론 FDA의 희귀의약품 지정(Orphan Drug Designation) 과정에서도 매우 귀중한 자료로 사용될 수 있을 것으로 기대한다”며 “현재 진행 중인 육종암 임상 성공적인 완료와 함께 미충족 의료수요가 높은 육종암 분야에서 가장 먼저 FDA허가 및 상용화를 목표로 개발에 박차를 가할 계획이다”고 말했다.